2025年11月03日
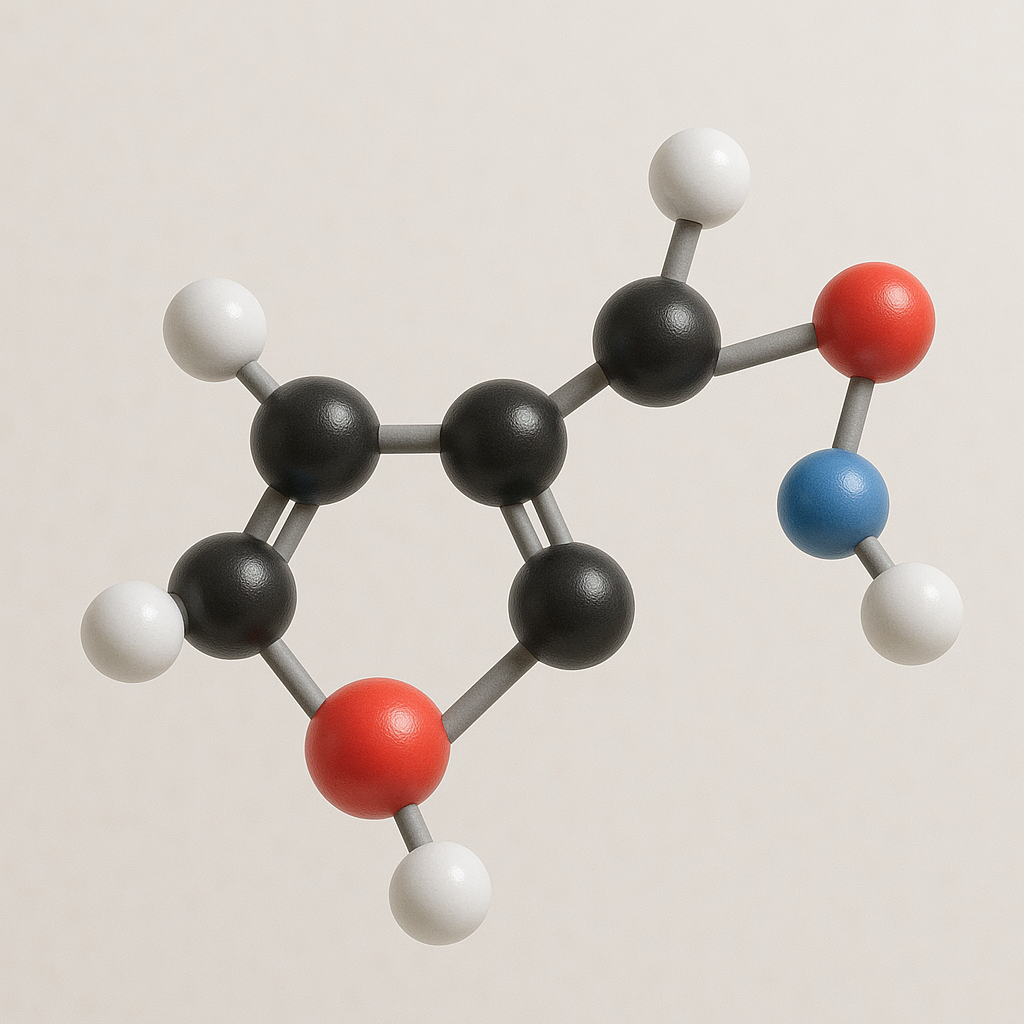
前回の記事では、ドーパミンの発見の歴史について学びました。今回は、ドーパミンの化学構造と、体内でどのように作られるのか(生合成)について詳しく解説します。
「化学」と聞くと難しそうに感じるかもしれませんが、ドーパミンの構造を理解することで、なぜこの物質が脳で重要な働きをするのか、そしてなぜ特定の病気と関連するのかが見えてきます。
化学式と系統名
ドーパミンはカテコールアミンという化学物質のグループに属します。その化学式はC₆H₃(OH)₂-CH₂-CH₂-NH₂で、正式な系統名は「4-(2-アミノエチル)ベンゼン-1,2-ジオール」です[7]。
難しい名前ですが、この名前から構造が分かります。
簡単に言うと:「ベンゼン環(六角形の炭素の輪)に、2つのOH(ヒドロキシル基)と、アミノ基(NH₂)がくっついた構造」です。
カテコール構造とは
ドーパミンの分子は、カテコール構造を持っています。これは、ベンゼン環(炭素6個が六角形に並んだ構造)に2つのヒドロキシル基(–OH)が隣り合って結合したものです[2][7]。

このカテコール構造に、エチル鎖(-CH₂-CH₂-)を介してアミン基(-NH₂)が結合しています。この構造により、ドーパミンはカテコールアミンファミリーの中で最もシンプルな分子となっています。
カテコールアミンファミリー
カテコールアミンファミリーには、以下の3つの重要な神経伝達物質が含まれます[2][7]:
- ドーパミン:最もシンプルな構造
- ノルアドレナリン(ノルエピネフリン):ドーパミンにOH基が1つ追加
- アドレナリン(エピネフリン):ノルアドレナリンにメチル基(-CH₃)が追加
これら3つの物質は構造が似ているため、体内では連続的に作られます。つまり、ドーパミンは他の2つの物質の「材料」でもあるのです。
材料は食べ物から
ドーパミンは、私たちが食事から摂取するアミノ酸を材料として作られます。具体的には、L-フェニルアラニンというアミノ酸が出発点となります[2][8]。

フェニルアラニンは「必須アミノ酸」の一つで、体内で作ることができないため、食事から摂取する必要があります。
含まれる食品:肉類、魚類、卵、大豆製品、乳製品、ナッツ類など、タンパク質が豊富な食品に多く含まれます。
ドーパミン生合成の4ステップ
ドーパミンは、以下の4つのステップを経て作られます[2][8]:
ステップ1:L-フェニルアラニン → L-チロシン
酵素:フェニルアラニンヒドロキシラーゼ
まず、食事から摂取したL-フェニルアラニンが、L-チロシンに変換されます。この反応には、フェニルアラニンヒドロキシラーゼという酵素が必要です[2]。
- 必要な補因子:分子状酸素(O₂)、テトラヒドロビオプテリン
- 反応の本質:ベンゼン環にOH基を1つ追加
豆知識:この酵素が欠損している遺伝性疾患が「フェニルケトン尿症」です。新生児マススクリーニングで検査されており、早期発見・治療により正常な発達が可能です。
ステップ2:L-チロシン → L-DOPA
酵素:チロシンヒドロキシラーゼ
次に、L-チロシンがL-DOPA(L-ジヒドロキシフェニルアラニン)に変換されます。この反応はチロシンヒドロキシラーゼという酵素によって触媒されます[2][8]。
このステップが律速段階です!つまり、ドーパミン生合成全体の速度を決めるのがこのステップです。チロシンヒドロキシラーゼの活性が高いほど、ドーパミンがたくさん作られます[2]。
- 必要な補因子:分子状酸素(O₂)、テトラヒドロビオプテリン、鉄(Fe²⁺)
- 反応の本質:ベンゼン環にもう1つOH基を追加(カテコール構造の完成)
ステップ3:L-DOPA → ドーパミン
酵素:DOPAデカルボキシラーゼ(芳香族L-アミノ酸デカルボキシラーゼ)
最後に、L-DOPAから二酸化炭素(CO₂)が取り除かれ、ドーパミンが生成されます。この反応はDOPAデカルボキシラーゼという酵素によって触媒されます[2][8]。
- 必要な補因子:ピリドキサールリン酸(ビタミンB6由来)
- 反応の本質:カルボキシル基(-COOH)が外れてCO₂として放出
パーキンソン病の治療で使われる「L-DOPA(レボドパ)」は、このステップの直前の物質です。
なぜL-DOPAを投与?ドーパミン自体は血液脳関門を通過できませんが、L-DOPAは通過できます。脳内でL-DOPAがドーパミンに変換され、不足分を補います[20]。
生合成のまとめ
ドーパミン生合成をまとめると:
L-フェニルアラニン(食事)
↓ フェニルアラニンヒドロキシラーゼ
L-チロシン
↓ チロシンヒドロキシラーゼ(★律速段階)
L-DOPA
↓ DOPAデカルボキシラーゼ
ドーパミン
ドーパミンは終点ではない
ドーパミンは、それ自体が重要な神経伝達物質ですが、さらに他の物質の「材料」でもあります。ドーパミンからは、ノルアドレナリンとアドレナリンが作られます[2][7]。
ドーパミン → ノルアドレナリン
酵素:ドーパミンβ-ヒドロキシラーゼ
ドーパミンは、ドーパミンβ-ヒドロキシラーゼという酵素によって、ノルアドレナリン(ノルエピネフリン)に変換されます[2][7]。
- 必要な補因子:分子状酸素(O₂)、L-アスコルビン酸(ビタミンC)、銅(Cu⁺)
- 反応の本質:エチル鎖の末端にOH基を追加
- 場所:主に神経末端の小胞内
ノルアドレナリンは、覚醒、注意、ストレス反応などに関わる神経伝達物質です。
ノルアドレナリン → アドレナリン
酵素:フェニルエタノールアミンN-メチルトランスフェラーゼ(PNMT)
さらに、ノルアドレナリンは、PNMTという酵素によって、アドレナリン(エピネフリン)に変換されます[2][7]。
- 必要な補因子:S-アデノシル-L-メチオニン(SAM)
- 反応の本質:アミン基にメチル基(-CH₃)を追加
- 場所:主に副腎髄質
アドレナリンは、緊急時の「闘争・逃走反応」を引き起こすホルモンです。
この一連の酵素反応により、1つのアミノ酸(フェニルアラニン)から、3つの重要な神経伝達物質(ドーパミン、ノルアドレナリン、アドレナリン)が作られるという、体内の効率的なシステムが明らかになります[2][7]。
なぜ調節が必要なのか
ドーパミンの量は、多すぎても少なすぎても問題を引き起こします。そのため、体内では生合成を厳密に調節する仕組みが備わっています。
主な調節メカニズム
1. フィードバック阻害
ドーパミン自体が、チロシンヒドロキシラーゼ(律速酵素)の活性を抑制します。つまり、ドーパミンが十分にあるときは、それ以上作らないようにブレーキがかかります。
例:車の速度制御装置のように、「目標速度に達したら、これ以上アクセルを踏まない」という仕組みです。
2. 酵素のリン酸化
神経活動が活発になると、チロシンヒドロキシラーゼがリン酸化(リン酸基が結合すること)され、活性が高まります。これにより、需要に応じてドーパミン産生が増加します。
3. 補因子の利用可能性
生合成に必要な補因子(テトラヒドロビオプテリン、ビタミンB6、ビタミンCなど)の量も、ドーパミン産生に影響します。
栄養状態がドーパミン産生に影響する理由がここにあります。
例:ビタミンB6(ピリドキシン)が不足すると、DOPAデカルボキシラーゼの活性が低下し、ドーパミン産生が減少する可能性があります。
遺伝的要因
ドーパミン生合成酵素の遺伝子に変異があると、ドーパミン産生に異常が生じることがあります。これが一部の神経精神疾患の発症に関与している可能性があります。
監修・執筆者
片山 渚 医師
五反田ストレスケアクリニック院長
- ✓ 精神保健指定医
- ✓ 日本医師会認定産業医
- ✓ 産業保健法務主任者(メンタルヘルス法務主任者)
- ✓ 健康経営アドバイザー
大学病院から民間病院まで幅広い臨床経験を活かし、患者さんが安心して治療を継続できるよう、わかりやすい情報提供を心がけています。
免責事項
本記事は一般的な情報提供を目的としており、特定の症状や状況に対する医学的アドバイスではありません。医療に関する決定は、必ず医師と相談の上で行ってください。本記事の情報に基づいて被ったいかなる損害についても、当院は責任を負いかねます。
- [7] Dopamine Biochemistry – News-Medical.Net
- [8] The Role of Dopamine as a Neurotransmitter in the Human Brain